Cadmiumsulfid
Cadmiumsulfid ist eine chemische Verbindung aus Cadmium und Schwefel. Es gehört zur Gruppe der II-VI-Verbindungshalbleiter.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 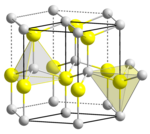
| ||||||||||||||||
| Kristallstrukturen von Hawleyit und Greenockit | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Cadmiumsulfid | |||||||||||||||
| Andere Namen |
Cadmiummonosulfid | |||||||||||||||
| Verhältnisformel | CdS | |||||||||||||||
| Kurzbeschreibung |
zitronengelbe, hexagonale (α-Form) oder scharlachrote, kubische (β-Form) Kristalle, gelbbraun als amorphes Pulver[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 144,48 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte | ||||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Sublimationspunkt |
980 °C[2] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Zulassungsverfahren unter REACH |
besonders besorgniserregend: krebserzeugend (CMR), ernsthafte Auswirkungen auf die menschliche Gesundheit gelten als wahrscheinlich[4] | |||||||||||||||
| MAK |
aufgehoben, da cancerogen[2] | |||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Vorkommen
BearbeitenCadmiumsulfid kommt in Form der Minerale Hawleyit und Greenockit in der Natur vor.
Darstellung
BearbeitenIm Labor wird feinteiliges Cadmiumsulfid der kubischen Modifikation durch Fällung einer heißen angesäuerten wässrigen Lösung von Cadmiumsulfat mit Schwefelwasserstoff erhalten:[6]
Aus Cadmiumhalogenidlösungen hingegen wird durch Schwefelwasserstofffällung die hexagonale Modifikation erhalten.
Eigenschaften
BearbeitenCadmiumsulfid ist ein Feststoff und kann als gelbe bis orangefarbene Kristalle (Wurtzit-Struktur), als gelbbraunes Pulver (amorphes Cadmiumsulfid) oder als scharlachrote kubische Kristalle (beta-Cadmiumsulfid) vorliegen. Cadmiumsulfid ist nicht brennbar und unlöslich in Wasser. Beim Erhitzen an der Luft erfolgt Zersetzung unter Bildung von Cadmiumoxid und Schwefeldioxid. Cadmiumsulfid weist bei einer Wellenlänge von 520 nm die maximale Empfindlichkeit auf.
Toxikologie
BearbeitenCadmiumsulfid wird von der EU-Liste nach dem GHS-System allgemein wie alle löslichen Cadmiumverbindungen eingestuft, obwohl das toxische Potenzial wesentlich geringer ist. Wasserlösliche Cadmiumverbindungen gelten im Allgemeinen als lungenschädigend, karzinogen, keimzellmutagen, reprotoxisch und gewässergefährdend, weil die löslichen Ionen leicht von den Lebewesen aufgenommen werden können. Cadmiumsulfid ist nicht wasserlöslich und chemisch relativ beständig. Die Zuordnung nach GHS erfolgt (momentan) aufgrund dieser allgemeinen Vorschrift für Cadmiumverbindungen. Eine toxikologische Einzelbeurteilung des Cadmiumsulfids liegt momentan nicht vor. Bei Schweiß- oder Lötarbeiten an mit Cadmiumsulfid behandelten Baumaterialien aus Altlasten wird stark toxischer Cadmiumoxid-Rauch freigesetzt.
Geschichte der Verwendung
BearbeitenFriedrich Stromeyer entdeckte das Cadmiumsulfid 1818 im Laboratorium. Es entsteht aus einer Fällung von Cadmiumsalzen und Schwefelwasserstoff oder Sulfiden. Die Verwendung als gelbes Pigment war lange Zeit üblich. Quecksilberanteile erzeugten eine rote Färbung. Cadmiumsulfid wird heute nicht mehr als Pigment eingesetzt, auch der Einsatz von Quecksilber ist nicht mehr erlaubt. Cadmiumsulfid wurde früher in Halbleitertechnik, Fotowiderständen oder in Leuchtstoffen für Fernsehröhren eingesetzt.[1] Auch als Bestandteil medizinischer Haarwaschmittel fand es Verwendung.[7]
Abbau
BearbeitenDer Abbau von Cadmiumsulfid auf historischen Ölgemälden erfolgt unter Lichteinfluss durch Oxidation zu Sulfat, wie durch Koen Janssens nachgewiesen wurde.[8] Auf den Gemälden konnte an Stelle der ursprünglichen gelben Pigmente farbloses CdSO4 · 2 H2O und (NH4)2Cd(SO4)2 gefunden werden.
Literatur
Bearbeiten- I. Fiedler, M. A. Bayard: Cadmium Yellows, Oranges and Reds. In: Artists’ Pigments. A Handbook of Their History and Characteristics. Vol. 1, Feller, R.L. (Ed.) Oxford University Press, 1986, S. 65–108 (Digitalisat).
Weblinks
Bearbeiten- Kremer-Pigmente: Cadmium-Farben, abgerufen am 20. März 2010.
- Cadmium yellow bei ColourLex
Einzelnachweise
Bearbeiten- ↑ a b c Eintrag zu Cadmiumsulfid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 10. Dezember 2014.
- ↑ a b c d e f g h Eintrag zu Cadmiumsulfid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ Eintrag zu Cadmium sulphide im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Eintrag in der SVHC-Liste der Europäischen Chemikalienagentur, abgerufen am 18. Oktober 2015.
- ↑ Datenblatt Cadmiumsulfid bei Alfa Aesar, abgerufen am 19. Mai 2007 (Seite nicht mehr abrufbar).
- ↑ Georg Brauer: Kadmiumsulfid. In: Handbuch der Präparativen Anorganischen Chemie. Ferdinand Enke Verlag, Stuttgart 1954, S. 813–814.
- ↑ Braun-Falco, O., Burg, G. (Hrsg.): Fortschritte der praktischen Dermatologie und Venerologie, Vorträge der X. Fortbildungswoche der Dermatologischen Klinik und Poliklinik der Ludwig-Maximilians-Universität München in Verbindung mit dem Berufsverband der Deutschen Dermatologen e. V. vom 25.–29. Juli 1983. Band 10. Springer-Verlag Berlin Heidelberg GmbH, 1983, S. 95.
- ↑ G. van der Snickt, J. Dik, M. Cotte, K. Janssens, J. Jaroszewicz, W. de Nold, J. Groenewegen, L. van der Loeff: Characterization of a Degraded Cadmium Yellow (CdS) Pigment in an Oil Painting by Means of Synchrotron Radiation Based X-ray Techniques. In: Analytical Chemistry. Band 81, Nr. 7, 2009, S. 2600–2610, doi:10.1021/ac802518z.


