4-Chlormercuribenzoesäure
chemische Verbindung
4-Chlormercuribenzoesäure ist eine organische Quecksilber-Verbindung, die als Protease-Inhibitor vor allem in der Biochemie Anwendung findet.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
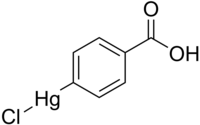
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 4-Chlormercuribenzoesäure | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C7H5ClHgO2 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 357,16 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Biochemische Eigenschaften
BearbeitenPCMB reagiert mit SH-Gruppen (Thiolgruppen) in Proteinen und ist somit ein Inhibitor für Enzyme, die abhängig sind von einer SH-Reaktivität. Es inhibiert die Cystein-Protease Papain, aber auch die Acetylcholinesterase von Säugetieren.
Verwendung
BearbeitenAufgrund seiner SH-Reaktivität wird es in speziellen Titrationen zur Quantifizierung von Thiolgruppen in Proteinen verwendet.
Quellen
Bearbeiten- ↑ a b c d Datenblatt 4-Chloromercuribenzoic acid bei Sigma-Aldrich, abgerufen am 18. März 2011 (PDF).
- ↑ Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag organic compounds of mercury with the exception of those specified elsewhere in this Annex im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.


