Dihydraziniumsulfat
Dihydraziniumsulfat ist eine anorganische chemische Verbindung aus der Gruppe der Hydrazinsalze.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
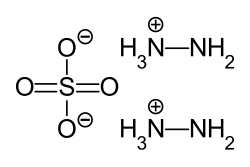
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Dihydraziniumsulfat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | (N2H5)2SO4 | ||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff mit süßlichem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 162,19 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
sehr leicht löslich in Wasser (2020 g·l−1 bei 20 °C)[1] und Ethanol[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Gewinnung und Darstellung
BearbeitenDihydraziniumsulfat kann durch Reaktion von Hydrazin mit Schwefelsäure gewonnen werden.[2]
Eigenschaften
BearbeitenDihydraziniumsulfat ist ein hygroskopischer, kristalliner, weißer bis naturweißer Feststoff mit süßlichem Geruch, der sehr leicht löslich in Wasser ist. Er zersetzt sich bei Erhitzung über 180 °C, wobei Ammoniak, Wasserstoff und Hydrazin entstehen.[1] Die Verbindung besitzt eine monokline Kristallstruktur mit der Raumgruppe P21/c (Raumgruppen-Nr. 14).[2]
Verwendung
BearbeitenDihydraziniumsulfat wird als Ausgangsstoff zur Herstellung von Kupferdihydraziniumsulfat (einem Fungizid) verwendet.[3]
Einzelnachweise
Bearbeiten- ↑ a b c d e f g h Eintrag zu Dihydraziniumsulfat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. April 2020. (JavaScript erforderlich)
- ↑ a b c Rune Liminga, Jan-Olof Lundgren u. a.: Hydrogen Bond Studies. 8. The Crystal Structure of Dihydrazinium Sulphate, (N2H5)2SO4. In: Acta Chemica Scandinavica 1947–1999. 19, 1965, S. 1612, doi:10.3891/acta.chem.scand.19-1612.
- ↑ Richard Wegler: Chemie der Pflanzenschutz- und Schädlingsbekämpfungsmittel Band 2: Fungizide · Herbizide · Natürliche Pflanzenwuchsstoffe · Rückstandsprobleme. Springer-Verlag, 1970, ISBN 978-3-7091-4184-7, S. 48 (eingeschränkte Vorschau in der Google-Buchsuche).


