Kaliumiodat
Kaliumiodat ist das Kalium-Salz der Iodsäure. Der weiße, kristalline Feststoff ist brandfördernd und kann als Oxidationsmittel eingesetzt werden.
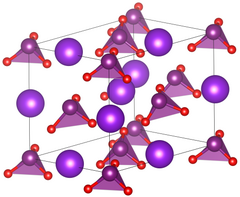
| Kristallstruktur | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||
| _ K+ _ I5+ _ O2− | ||||||||||||||||||||||
| Kristallsystem |
triklin | |||||||||||||||||||||
| Raumgruppe |
P1 (Nr. 1) | |||||||||||||||||||||
| Gitterparameter |
a = 8,923 Å, b = 8,942 Å, c = 7,709 Å, α = 54,4°, β = 125,3°, γ = 90,6° | |||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Kaliumiodat | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Verhältnisformel | KIO3 | |||||||||||||||||||||
| Kurzbeschreibung |
weißer, kristalliner Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 214,00 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte |
3,98 g·cm−3[1] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
mäßig in Wasser (92 g·l−1 bei 25 °C)[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Herstellung
BearbeitenIodate können aus Iod und heißer Alkalilauge gewonnen werden. So entsteht Kaliumiodat aus Iod und heißer Kalilauge:
Diese Reaktion ist analog der Herstellung von Chloraten aus Chlor und heißer Lauge.
Eigenschaften und Verwendung
BearbeitenKaliumiodat bildet farblose Kristalle, die in Wasser nur mäßig löslich sind. Die Löslichkeit erhöht sich mit steigender Temperatur.[3]
| Löslichkeit von Kaliumiodat in Wasser[3] | ||||||||||||
| Temperatur | in °C | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 100 | |||
| Konzentration | in g/100 g H2O | 4,60 | 6,27 | 8.08 | 10,3 | 12,6 | 18,3 | 24,80 | 32,3 | |||
Iodate sind ausgesprochen gute Oxidationsmittel. Wenn ihre Lösungen angesäuert werden, liegen sie im Gleichgewicht mit ihrer Säure vor; die Lösung wirkt dann stark oxidierend, wobei das Oxidationspotential +1,196 V beträgt. Mit Iodid reagieren Iodate in saurer Lösung zum Iod, es findet also eine Komproportionierung statt:
Diese Reaktion ist eine Teilreaktion der Landolt-Reaktion, bei der ein Farbumschlag erst nach einer bestimmten Zeit erfolgt und bei der bevorzugt Kaliumiodat eingesetzt wird.
Bei Zimmertemperatur liegt Kaliumiodat in einer triklinen Struktur vor. Diese hat die Raumgruppe P1 (Raumgruppen-Nr. 1) mit den Gitterparametern a = 8,923 Å, b = 8,942 Å, c = 7,709 Å, α = 54,4°, β = 125,3°, γ = 90,6°. Bei 72,5 °C geht diese in eine monokline Struktur mit der Raumgruppe Cm (Nr. 8), bei 212 °C in eine trigonale Struktur mit der Raumgruppe R3m (Nr. 166) über.[4]
Die wichtigsten Anwendungen von Kaliumiodat liegen in der analytischen Chemie, wo es auch als Urtiter verwendet wird.
Iodiertes Speisesalz enthält ca. 20 ppm Kalium- oder Natriumiodat (0,020 mg/g)[5]. Kaliumiodid lässt sich hierzu nicht verwenden, da es zu leicht oxidiert werden kann. Medizinische Jodmangel-Tabletten enthalten etwa den empfohlenen Tagesbedarf, rund 0,1 mg/Stück. Spezielle Strahlenschutz-Jodtabletten sind dagegen mit rund 100 mg/Stück um den Faktor 1000 höher dosiert.
Sicherheitshinweise
BearbeitenIodate sind als starke Oxidationsmittel von Reduktionsmitteln wie Schwefel, Metallpulvern oder organischen Substanzen fernzuhalten. Im Tierversuch mit Kaninchen zeigte Kaliumiodat starke Reizwirkungen auf die Augen und die Haut.[6]
Einzelnachweise
Bearbeiten- ↑ a b c d Datenblatt Kaliumiodat bei Merck, abgerufen am 15. August 2010.
- ↑ Eintrag zu Kaliumiodat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ a b Dean, J.A.: Lange's Handbook of Chemistry, 15. Ed. 1999, McGraw-Hill, Inc. New York, ISBN 0-07-016384-7.
- ↑ S.A. Hamid: Symmetrie von KIO3 und die Struktur der Zimmertemperaturphase. In: Zeitschrift für Kristallographie, Kristallgeometrie, Kristallphysik, Kristallchemie, 137, 1973, S. 412–421, doi:10.1524/zkri.1973.137.16.412.
- ↑ Eintrag zu iodiertes Speisesalz. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. April 2016.
- ↑ Datenblatt Kaliumiodat bei Alfa Aesar, abgerufen am 15. August 2010 (Seite nicht mehr abrufbar).

