Perfluorbutansäure
Perfluorbutansäure ist eine chemische Verbindung aus der Gruppe der Perfluorcarbonsäuren.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
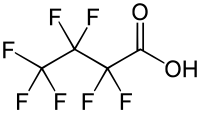
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Perfluorbutansäure | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C4HF7O2 | ||||||||||||||||||
| Kurzbeschreibung |
hellgelbe stinkende Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 214,04 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[2] | ||||||||||||||||||
| Dichte |
1,645 g·cm−3 (25 °C)[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
120 °C (755 mmHg)[2] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
mischbar mit Wasser, Toluol, Diethylether, Ethanol und Benzol[1] | ||||||||||||||||||
| Brechungsindex |
1,3082 (20 °C)[4] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Gewinnung und Darstellung
BearbeitenPerfluorbutansäure kann durch Elektrofluorierung von Buttersäure gewonnen werden.[5]
Eigenschaften
BearbeitenPerfluorbutansäure ist eine hellgelbe stinkende Flüssigkeit, die mischbar mit Wasser, Toluol, Diethylether, Ethanol und Benzol ist.[1] Von PFBA gibt es zwei Strukturisomere.[6]
Verwendung
BearbeitenPerfluorbutansäure ist ein Ionenpaar-Reagenz für die Umkehrphasen-HPLC. Es wird bei der Sequenzierung, Synthese und Solubilisierung von Proteinen und Peptiden[7] sowie als mobiler Phasenmodifikator zur Erhöhung der Selektivität bei der HPLC-Analyse von Histonproteinen verwendet. Es ist ein wirksames Additiv für die galvanische Zinkabscheidung.[1]
Laut Angaben der chemischen Industrie handelt es sich bei der Perfluorbutansäure um eine von 256 per- und polyfluorierter Alkylverbindungen mit kommerzieller Relevanz[8][9] aus der OECD-Liste von 4730 PFAS.[10]
Auswirkungen
BearbeitenEine Studie an 323 COVID-19-Patienten ergab, dass eine erhöhte Konzentration von Perfluorbutansäure im Körper mit einem gesteigerten Risiko eines schwereren Verlaufs einer COVID-19-Infektion korreliert ist.[11][12]
Die PFBA-Konzentration in Eisbohrkernen vom Devon Ice Cap und dem Mt.-Oxford-Eisfeld aus der kanadischen Arktis stieg von etwa 1985 bis 2010 stark an.[13]
Einzelnachweise
Bearbeiten- ↑ a b c d e Datenblatt Heptafluorobutyric acid, 99% bei Alfa Aesar, abgerufen am 4. September 2020 (Seite nicht mehr abrufbar).
- ↑ a b c d e Datenblatt Heptafluorobutyric acid, ≥99.0% (GC) bei Sigma-Aldrich, abgerufen am 4. September 2020 (PDF).
- ↑ Datenblatt Heptafluorbuttersäure bei Merck, abgerufen am 4. September 2020.
- ↑ Groth, R. H.: Fluorinated paraffins. In: Journal of Organic Chemistry. Band 24, 1959, S. 1709–1715, doi:10.1021/jo01093a022.
- ↑ Houben-Weyl Methods of Organic Chemistry Vol. V/3, 4th Edition Fluorine and Chlorine Compounds. Georg Thieme Verlag, 2014, ISBN 3-13-179994-3, S. 45 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Sierra Rayne, Kaya Forest, Ken J. Friesen: Congener-specific numbering systems for the environmentally relevant C4 through C8 perfluorinated homologue groups of alkyl sulfonates, carboxylates, telomer alcohols, olefins, and acids, and their derivatives. In: Journal of Environmental Science and Health, Part A. Band 43, Nr. 12, 12. September 2008, S. 1391–1401, doi:10.1080/10934520802232030.
- ↑ Hubert Rehm, Thomas Letzel: Der Experimentator: Proteinbiochemie/Proteomics. Springer-Verlag, 2016, ISBN 978-3-662-48851-5, S. 257 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Robert C. Buck, Stephen H. Korzeniowski, Evan Laganis, Frank Adamsky: Identification and Classification of Commercially Relevant Per- and Poly-fluoroalkyl Substances (PFAS). In: Integrated Environmental Assessment and Management. doi:10.1002/ieam.4450.
- ↑ There’s no need to control PFAS as a class, industry scientists say. In: Chemical & Engineering News. 19. Mai 2021, abgerufen am 10. April 2022.
- ↑ Toward a New Comprehensive Global Database of Per- and Polyfluoroalkyl Substances (PFASs): Summary Report on Updating the OECD 2007 List of Per- and Polyfluoroalkyl Substances (PFASs) (= OECD Series on Risk Management of Chemicals. Nr. 39). OECD, 2018, ISBN 978-92-64-88443-4, doi:10.1787/1a14ad6c-en.
- ↑ PFAS exposure linked with worse COVID-19 outcomes. Harvard T.H. Chan School of Public Health, 5. Januar 2021, abgerufen am 4. Februar 2021 (amerikanisches Englisch).
- ↑ Philippe Grandjean, Clara Amalie Gade Timmermann, Marie Kruse, Flemming Nielsen, Pernille Just Vinholt: Severity of COVID-19 at elevated exposure to perfluorinated alkylates. In: PLOS ONE. Band 15, Nr. 12, 31. Dezember 2020, S. e0244815, doi:10.1371/journal.pone.0244815, PMID 33382826, PMC 7774856 (freier Volltext).
- ↑ Heidi M. Pickard, Alison S. Criscitiello, Daniel Persaud, Christine Spencer, Derek C. G. Muir, Igor Lehnherr, Martin J. Sharp, Amila O. De Silva, Cora J. Young: Ice Core Record of Persistent Short‐Chain Fluorinated Alkyl Acids: Evidence of the Impact From Global Environmental Regulations. In: Geophysical Research Letters. Band 47, Nr. 10, 28. Mai 2020, doi:10.1029/2020GL087535.
