Pomarose
Pomarose ist ein hoch-intensiver, von Givaudan patentierter[3] captiver Riechstoff. Pomarose, ein zweifach ungesättigtes Keton, das nicht in der Natur vorkommt, besitzt einen sehr starken, fruchtigen Rosengeruch mit Anklängen an Äpfel, Pflaumen und Rosinen, der fast ausschließlich auf das (2E,5Z)-Stereoisomer zurückgeht. Das (2E,5E)-konfigurierte Isomer ist dagegen für die meisten Leute geruchlos.[4] Bereits geringste Säurespuren reichen allerdings zur cis-trans-Equilibrierung der C-5-Doppelbindung aus, was etwa schon beim längeren Stehen in Glasgefäßen beobachtet wird.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
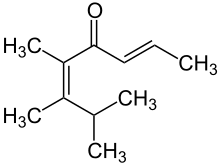
| |||||||||||||
| Allgemeines | |||||||||||||
| Name | Pomarose | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C11H18O | ||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit intensivem fruchtig-rosigem an Apfelkuchen, Pflaumen und Trockenfrüchte erinnernden Geruch[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 166,26 g·mol−1 | ||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Entdeckung und Synthese
BearbeitenBei der Analyse von NMR-Spekten hielten Philip Kraft und Mitarbeiter[5] 5,6,7-Trimethylocta-2,5-dien-4-on anfangs für eine unbekannte Spurenkomponente mit Damascongeruch in einem komplexen Reaktionsgemisch. Die besagte Spurenkomponente dieses Gemisches stellte sich allerdings bald als das konstitutionsisomere 2-Methyl-3-isopropylhepta-2,5-dien-4-on heraus, das in der Tat auch einen Damascongeruch besitzt. Aus reiner Kuriosität an den Struktur–Geruchs-Beziehungen dieser Verbindung wurde dann aber auch 5,6,7-Trimethylocta-2,5-dien-4-on (Pomarose) synthetisiert, und erwies sich überraschend als parfümistischer Volltreffer mit strahlend fruchtiger Rosen-Note, die daneben auch an Apfelkuchen, Pflaumen und Trockenfrüchte erinnerte. Darüber hinaus besaß sie einen niedrigen Geruchsschwellenwert von nur 0,5 ng/l Luft. Die Synthese bestand aus Bortrifluorid-katalysierte Addition von Methylisopropyl-Keton an 1-Ethoxyprop-1-in zum 2,3,4-Trimethylpent-2-ensäureethylester, welcher dann anschließend durch Grignard-Reaktion mit Propen-1-ylmagnesiumbromid unter In-situ-Enolisierung in das Zielmolekül übergeführt wurde.
Verwendung in der Parfümerie
BearbeitenPomarose hatte sein Debüt mit 0,36 % in „Be Delicious for Men“ von Olivier Gillotin und Pierre Negrin.[6] Der DKNY-Parfümbrief suchte nach einem Duft für 'einen bestimmt wirkenden, weltgewandten Mann, der für alles offen ist, was das Leben im Big Apple von New York zu bieten hat'. In diesem Zusammenhang passte das Apfel-Rose-Thema von Pomarose perfekt, so dass das Parfüm um diesen Riechstoff herum kreiert wurde. Nur ein Jahr später, wurde Pomarose mit 0,43 % in „Unforgivable“ (Sean John, 2006) in einem Champagner-Akkord von David Apel, Pierre Negrin, Caroline Sabas, und Aurélien Guichard überdosiert. In „1 Million“ (Paco Rabanne, 2008) stellen Christophe Raynaud, Olivier Pescheux und Michel Girard 0,18 % dieses extrem intensiven Riechstoffs einer hellen Ledernote gegenüber. Ellen Molner und Rodrigo Flores-Roux verwendeten Pomarose in dem aromatischen Fougère-Parfüm „CK free“ (Calvin Klein, 2009), und Olivier Pescheux kontrastierte den Eichenmoos-Riechstoff Evernyl mit Pomarose in „Legend“ (Mont Blanc, 2011). In der Damenparfümerie wurde Pomarose unter anderem von David Apel im Piña Colada-Akkcord von „Unforgivable Woman“ (Sean John, 2006) eingesetzt, und es findet sich auch als Bestandteil der 'Haarspray' Rosen-Note von „John Galliano“ (John Galliano, 2008).
Verwandte Riechstoffe
Bearbeiten- α- und β-Damascon
- Damascenone
Einzelnachweise
Bearbeiten- ↑ Günther Ohloff, Wilhelm Pickenhagen, Philip Kraft: Scent and Chemistry – The Molecular World of Odors. Helvetica Chimica Acta, Zurich 2012, ISBN 978-3-906390-66-6, S. 82 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Patent EP1149820: 2-,5-,6-,7-,8-substituted oct-2-ene-4-one. Angemeldet am 21. April 2001, Erfinder: Philip Kraft.
- ↑ Karl A. D Swift, Royal Society of Chemistry (Great Britain): Advances in flavours and fragrances : from the sensation to the synthesis. Royal Society of Chemistry, Cambridge 2002, ISBN 0-85404-821-9, S. 138 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Philip Kraft, Caroline Denis, Walter Eichenberger: 5,6,7-Trimethylocta-2,5-dien-4-one – A Suspected Odorant with Surprising Olfactory Properties. In: European Journal of Organic Chemistry. 2001. Jahrgang, Nr. 12, 2001, S. 2363–2369, doi:10.1002/1099-0690(200106)2001:12<2363::AID-EJOC2363>3.0.CO;2-E.
- ↑ Günther Ohloff, Wilhelm Pickenhagen, Philip Kraft: Scent and Chemistry – The Molecular World of Odors. Helvetica Chimica Acta, Zurich 2012, ISBN 978-3-906390-66-6, S. 217 (eingeschränkte Vorschau in der Google-Buchsuche).