Remimazolam
Remimazolam ist ein Arzneistoff aus der Gruppe der Benzodiazepine. Remimazolam wurde in Japan (als Anerem) im Januar 2020 zur allgemeinen Sedierung und in den USA und der EU (als Byfavo) im Juli 2020 bzw. März 2021 zur prozeduralen Kurzzeitsedierung (bei Verfahren, die bis zu 30 Minuten dauern) zugelassen.[2][3][4]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
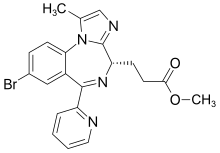
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Remimazolam | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C21H19BrN4O2 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code | ||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 439,31 g·mol−1 | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Es wird parenteral angewendet in Form des Benzolsulfonsäure-Salzes, Remimazolambesilat.[5]
Pharmakologische Eigenschaften
BearbeitenDer Wirkungsmechanismus gleicht dem anderer Benzodiazepine: Remimazolam bindet an GABAA-Rezeptoren im Gehirn. Wie andere Benzodiazepine zeigt auch Remimazolam keine deutliche Selektivität innerhalb der Subtypen des GABAA-Rezeptors. Die primäre Verstoffwechselung verläuft über Gewebscarboxyesterasen (hauptsächlich CES1) und weitgehend ohne Cytochrom-P450-abhängige Abbauwege. Der resultierende Metabolit CNS-7054[6] weist eine 300-fach geringere Affinität zum Rezeptor auf[4] und ist somit weitgehend inaktiv.
Remimazolam ist ultrakurz wirksam und hat eine terminale Plasmahalbwertszeit von 37 bis 53 Minuten, die mittlere Halbwertszeit der Verteilung (t1/2α) liegt zwischen 0,5 und 2 Minuten. Bei gesunden Probanden werden mindestens 80 % und bei Koloskopiepatienten 50 % bis 60 % der Dosis in Form des pharmakologisch inaktiven Metaboliten im Urin ausgeschieden.[4]
Nebenwirkungen
BearbeitenUnerwünschte Wirkungen wie verminderter Sauerstoffgehalt im Blut (Hypoxie), Minderung des Blutdrucks (Hypotonie) und der Herzschlagfrequenz (Bradykardie) erfordern die Überwachung während der Sedierung und in der Erholungsphase.
Studien
BearbeitenDie Zulassung erfolgte auf der Grundlage von Ergebnisse aus drei randomisierten, multizentrischen klinischen Studien (Studie 1/NCT02290873, Studie 2/NCT02296892 und Studie 3/NCT02532647) an 969 Erwachsenen, die sich kurzen Eingriffen unterzogen: Studien 1 und 3 wurden bei Teilnehmern durchgeführt, die sich einer Koloskopie, Studie 2 wurde bei Teilnehmern durchgeführt, die sich einer Bronchoskopie unterzogen. In den Studien wurden die Teilnehmer nach dem Zufallsprinzip in drei Gruppen eingeteilt: Eine Gruppe erhielt Remimazolam, eine Gruppe erhielt Placebo und eine Gruppe erhielt Midazolam (vergleichbares, bereits zugelassenes Medikament mit sedierender Wirkung). Die ersten beiden Gruppen wurden doppelblind behandelt, jeweils mit der Option, bei Bedarf zusätzlich Midazolam zu erhalten. In der dritten Gruppe erhielten alle Teilnehmer nur Midazolam.
In allen drei Studien erhielten die Teilnehmer zusätzlich ein Mittel zur Schmerzkontrolle.
Die Studien 1 und 2 verglichen die Teilnehmer, die Remimazolam erhielten, mit den Teilnehmern der anderen beiden Gruppen und maßen den Erfolg der Sedierung anhand der vorgegebenen Kriterien. Daten aus Studie 3 wurden in erster Linie verwendet, um die Nebenwirkungen von Remimazolam zu bewerten.[7]
Zulassung und Vermarktung
BearbeitenRemimazolam ist eine Entwicklung des Unternehmens Paion. Für die Vermarktung von Remimazolam in außereuropäischen Staaten arbeitet die Firma mit Partnern wie Acacia Pharma (USA), Mundipharma (J), R-Pharm (Russland/GUS, TR, MENA-Region) und anderen zusammen.[8]
Paion gibt an, auf der Basis von positiven Ergebnissen in Phase-3-Stdien auch in der EU eine Zulassungserweiterung für die Anwendung von Remimazolam in der Allgemeinanästhesie anzustreben.[8]
Handelsnamen
Anerem (J), Byfavo (USA, EU, UK, KOR), Ruima (CN)
Anwendung im Compassionate Use
Im Juni 2020 erhielt das lokale Ethikkomitee des Krankenhauses in Mailand die Genehmigung für den „Compassionate Use“ von Remimazolam zur Sedierung von Patienten mit schweren COVID-19-Verläufen. Die ansonsten häufig eingesetzten Wirkstoffe Midazolam und Propofol waren unter anderem auch in Kliniken in Italien knapp geworden.[9]
Weblinks
BearbeitenEinzelnachweise
Bearbeiten- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Novel Drug Approvals for 2020. FDA (englisch).
- ↑ Remimazolam: First Approval In: Drugs. 2020, doi:10.1007/s40265-020-01299-8. PMID 32274703.
- ↑ a b c BYFAVO- remimazolam besylate injection, powder, lyophilized, for solution. DailyMed (englisch).
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Remimazolambesilat: CAS-Nr.: 1001415-66-2, EG-Nr.: 811-733-8, ECHA-InfoCard: 100.242.468, PubChem: 23658607, ChemSpider: 30790854, DrugBank: DBSALT002953, Wikidata: Q27254247.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu CNS-7054: CAS-Nr.: 960305-91-3, PubChem: 46941174, ChemSpider: 32697517, Wikidata: Q27236793.
- ↑ Drug Trials Snapshots: BYFAVO. U.S. Food and Drug Administration, abgerufen am 26. Juli 2020.
- ↑ a b Paion erhält Zulassung der Europäischen Kommission für Byfavo(R) (Remimazolam) in der prozeduralen Sedierung. 27. März 2021.
- ↑ Statt Propofol und Midazolam: Klinik testet Remimazolam. In: Apotheke Adhoc. 2. Juni 2020 (apotheke-adhoc.de).